생명의 설계도라고 불리는 DNA는 오랫동안 ‘한 번 결정되면 바꿀 수 없는 숙명’으로 여겨져 왔습니다. 부모로부터 물려받은 유전적 코드가 건강과 성격, 심지어 노화의 속도까지 결정한다는 믿음은 생물학의 근간을 이뤘습니다.
그러나 2026년 3월, 최신 연구들은 이러한 고정관념을 완전히 뒤흔들고 있다. 과학자들은 이제 4억 년 전 식물이 숨겨둔 유전적 스위치를 찾아내고, 암세포를 공격하도록 면역 세포를 ‘터보차저’로 업그레이드하며, 심지어 DNA를 자르지 않고도 유전자의 기능을 끄고 켜는 정밀한 기술을 선보이고 있습니다.
마치 컴퓨터 소프트웨어를 업데이트하듯 우리의 생물학적 코드를 조정하는 시대가 도래한 것입니다.
유전학의 최전선에서 벌어지고 있는 이 흥미진진한 변화들은 단순히 질병을 치료하는 것을 넘어, 인류가 스스로의 진화적 경로를 재설계할 수 있는 가능성을 제시합니다.
유전자 재설계의 새시대
유전 공학은 이제 ‘자르고 붙이는’ 거친 편집의 시대를 지나, 유전자의 기능을 미세하게 조정하는 정밀 예술의 단계에 진입했습니다.
특히 2026년 3월에 발표된 연구들은 안전성과 효율성이라는 두 마리 토끼를 잡는 데 성공하며 임상 적용의 문턱을 크게 낮췄습니다.
CRISPR의 진화: 유전자 가위에서 ‘분자 빗자루’로
과거의 CRISPR 기술은 가위처럼 DNA를 직접 절단하여 유전자를 교정하는 방식을 사용했습니다.
하지만 DNA를 자르는 행위 자체가 세포에는 큰 스트레스를 주며, 예기치 못한 암 발생이나 대규모 게놈 결실의 위험을 내포하고 있었습니다.[1]
UNSW 시드니와 세인트 주드 어린이 연구 병원의 공동 연구팀은 이러한 위험을 획기적으로 줄인 ‘에피제네틱 편집(Epigenetic Editing)’ 기술을 선보였습니다.[1]
연구진은 DNA 서열 자체는 그대로 두면서, 유전자 표면에 붙어 있는 ‘메틸기’라는 화학적 표지만을 제거하거나 추가하여 유전자의 스위치를 조절하는 데 성공했습니다.[1]
이는 마치 책의 내용은 바꾸지 않으면서, 특정 페이지가 열리지 않도록 붙여놓은 포스트잇을 떼어내는 것과 같습니다.
이 기술은 특히 겸상 적혈구 빈혈증 치료에서 빛을 발하고 있는데, 태아 시절에만 활성화되던 ‘태아형 글로빈 유전자’의 잠금장치를 에피제네틱 편집으로 풀어내어 성인이 되어서도 정상적인 혈액 기능을 수행할 수 있게 합니다.[1]
개념 정리: DNA 메틸화(Methylation)란?
DNA 메틸화는 DNA 염기 서열의 사이토신(C)에 메틸기(CH3)가 결합하는 현상을 말합니다.
이는 유전자의 염기 서열을 바꾸지는 않지만, 전사 인자가 DNA에 결합하는 것을 방해하여 유전자 발현을 억제합니다.
포유류 게놈 라이팅: 10kb 이상의 거대 설계도 그리기
지금까지의 게놈 편집이 오타 하나를 고치는 수준이었다면, 이제는 문단 전체를 새로 쓰는 ‘게놈 라이팅(Genome Writing)’의 시대가 열리고 있습니다.[2]
2026년 3월에 발표된 종합 리뷰에 따르면, 과학자들은 이제 포유류 세포 내에 10kb(1만 개의 염기쌍) 이상의 거대 합성 DNA 세그먼트를 안정적으로 삽입하는 기술을 확보했습니다.[2]
이러한 기술은 단순히 질병을 치료하는 것을 넘어, 복잡한 유전적 회로를 갖춘 차세대 세포 치료제를 만들거나 인간의 생리 기능을 정밀하게 모방한 질병 모델을 구축하는 데 필수적입니다.[2]
특히 거대 유전자를 하향식(Top-down)이 아닌 상향식(Bottom-up)으로 설계하고 조립하여 통합하는 방식은 합성 생물학의 새로운 지평을 열었다고 볼 수 있다.[2]
| 기술 세대 | 핵심 메커니즘 | 주요 장점 | 주요 한계 및 도전 과제 | 출처 |
|---|---|---|---|---|
| 1세대 (CRISPR-Cas9) | DNA 이중 가닥 절단 (DSB) | 강력한 유전자 녹아웃 기능 | 오프 타겟 효과 및 암 위험 | [1] |
| 2세대 (Base/Prime Editing) | 단일 염기 치환 및 정밀 교정 | 절단 없는 정밀성 | 거대 유전자 삽입의 어려움 | [3] |
| 3세대 (Epigenetic Editing) | 화학적 마커(메틸기 등) 조절 | 서열 보존, 최고의 안전성 | 장기적인 발현 유지 기전 연구 필요 | [1] |
| 4세대 (Genome Writing) | 거대 합성 DNA 삽입 | 복잡한 유전 회로 구축 가능 | 전달 효율 및 게놈 안정성 확보 | [2] |
식물 게놈과 기후 변화
기후 변화로 인한 전 지구적 식량 위기는 인류가 직면한 가장 시급한 과제입니다.
2026년 3월, 식물 유전학자들은 식물의 게놈 속에 수억 년 동안 감춰져 있던 생존 전략을 해독하여 ‘기후 저항성 작물’을 개발하는 데 성공했습니다.
식물 속 230만 개의 ‘고대 스위치’ 발견
Science지에 발표된 콜드 스프링 하버 연구소(CSHL)의 연구는 식물 생물학계에 엄청난 충격을 주었습니다.[5]
연구진은 284종, 314개의 식물 게놈을 비교 분석한 결과, 무려 4억 년 전부터 보존되어 온 230만 개의 유전적 스위치를 발견했습니다.[5]
‘보존된 비부호화 서열(CNSs)’이라고 불리는 이 스위치들은 단백질을 직접 만들지는 않지만, 유전자가 언제, 어디서 활성화될지를 결정하는 사령탑 역할을 합니다.[5]
연구팀은 ‘Conservatory’라는 혁신적인 전산 도구를 개발하여, 꽃이 피는 식물이 나타나기 훨씬 이전부터 존재했던 고대의 스위치들을 찾아냈습니다.[5]
이들은 식물 유전체가 진화하는 과정에서 세 가지 핵심적인 규칙을 따른다는 사실을 밝혀냈습니다.
- 일관된 순서 유지: 염색체 상의 물리적 거리는 변할 수 있어도, 스위치들의 배치 순서는 수억 년 동안 일정하게 유지된다.[5]
- 재배열을 통한 새로운 연결: 게놈이 재배열되는 과정에서 고대의 스위치가 완전히 새로운 유전자와 연결되어 새로운 형질을 만들어낸다.[5]
- 유전자 중복 후의 지속성: 유전자가 복제된 후에도 이 스위치들은 사라지지 않고 남아, 유전자 가족의 진화를 이끄는 원동력이 된다.[5]
이 발견은 가뭄이나 병충해에 강한 새로운 작물을 육종하려는 과학자들에게 거대한 유전적 보물지도를 제공한 것과 같습니다.[5]
광합성 최적화: 루비스코의 치명적인 실수 바로잡기
식물 성장의 핵심인 광합성 과정에는 치명적인 설계 결함이 있습니다.
광합성에서 이산화탄소를 고정하는 루비스코(Rubisco) 효소는 가끔 산소를 잘못 잡아채는 실수를 저지르는데, 이로 인해 독성 부산물이 생성되고 이를 정화하는 과정에서 식물은 막대한 에너지를 낭비합니다.[6]
기온이 상승하면 루비스코의 실수는 더욱 잦아지며, 이는 주요 작물의 생산성을 20~30% 감소시키는 원인이 됩니다.[6]
PNAS에 보고된 RIPE(광합성 효율 증대) 프로젝트팀은 유전공학을 통해 이 에너지 낭비 경로를 차단하는 데 성공했습니다.[6]
이들은 담배와 감자를 모델로 하여, 루비스코의 실수로 생긴 부산물을 세포 내에서 더 효율적으로 분해하는 새로운 대사 경로를 설계했습니다.[6]
일리노이주의 실제 노지 실험 결과, 이렇게 엔지니어링된 작물은 고온 환경에서도 야생형보다 생산성이 최대 26% 이상 높게 나타났습니다.[6]
이는 기후 온난화 시대에 식량 안보를 지킬 수 있는 강력한 무기가 될 것으로 보입니다.
| 작물 종류 | 연구 성과 | 생산성 향상 비율 (고온 조건) | 주요 기전 | 출처 |
|---|---|---|---|---|
| 담배 (모델 식물) | 광호흡 경로 우회 설계 | 약 26% | 루비스코 부산물 효율적 분해 | [6] |
| 감자 | RIPE 기술 적용 성공 | 7.5% ~ 30% | 대사 경로 최적화 및 철분 함량 증가 | [6] |
| 벼 (Rice) | OsCBL4-CIPK signaling | 삼투압 스트레스 저항성 향상 | 염분 및 탈수 대응 신호 모듈 강화 | [7] |
| 애기장대 | Hsp70 과발현 | 열 저항성 획기적 증가 | 열 충격 단백질을 통한 세포 보호 | [6] |
[과학쏙쏙] 루비스코란?
루비스코는 지구상에서 가장 풍부한 단백질로 알려져 있으며, 무기 탄소($CO_2$)를 유기물로 전환하는 첫 번째 단계를 담당합니다.
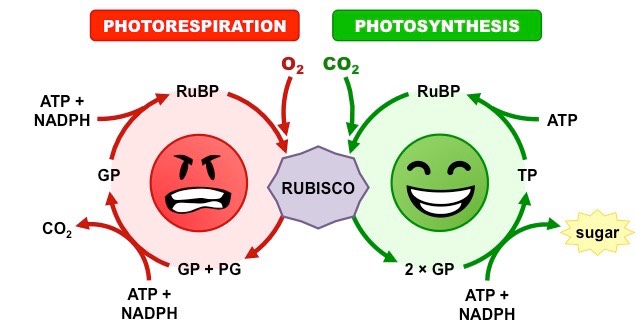
- 반응의 이중성: 루비스코는 두 가지 반응을 동시에 촉매합니다. 1. 카르복실화(Carboxylation): RuBP + CO₂ → 2*3-PGA (광합성 과정) 2. 산소화(Oxygenation): RuBP + O₂ → 3-PGA + 2-Phosphoglycolate (광호흡 과정)
- 구조적 특징: 고등 식물의 루비스코는 대단위체(Large subunit, L) 8개와 소단위체(Small subunit, S) 8개로 구성된 복합체 형태를 띱니다. 대단위체는 엽록체 게놈(rbcL)에, 소단위체는 핵 게놈(rbcS)에 암호화되어 있습니다.
- 낮은 효율성: 효소치고는 대단히 느립니다. 일반적인 효소가 초당 수천 개의 분자를 처리할 때, 루비스코는 초당 고작 3~10개의 CO₂ 분자만을 처리합니다. 식물이 이 낮은 효율을 극복하기 위해 선택한 전략은 ‘물량 공세’입니다. 잎 단백질의 약 30~50%가 루비스코입니다.
작물 탄력성을 위한 유전체 네트워크 분석
현대 농학은 단순히 개별 유전자를 조작하는 단계를 넘어, 유전자들 사이의 복잡한 네트워크를 이해하는 방향으로 나아가고 있습니다.
벼(Oryza sativa)를 포함한 주요 화본과 식물 5종에 대한 전 게놈 분석 연구에서는, 삼투압 스트레스에 반응하는 핵심 신호 전달 모듈인 CBL과 CIPK 유전자 가족의 진화 과정이 밝혀졌습니다.[7]
연구에 따르면, 특히 OsCBL4 유전자는 전통적으로 염분 스트레스 센서로 알려져 있었으나, 최신 분석 결과 탈수 반응에 특화된 시스-엘리먼트(cis-element) 구조를 가지고 있음이 확인되었습니다.[7]
이는 가뭄 조건에서 식물이 어떻게 수분 손실을 감지하고 대응하는지를 분자 수준에서 보여주는 사례입니다.
또한, 이러한 신호 전달 유전자들은 분절 복제(Segmental duplication)를 통해 확장되어 왔으며, 이는 식물이 가혹한 환경 변화에 적응해 온 유전적 전략임을 시사합니다.[7]
3차원 유전체 구조: 생명의 시작과 질병의 경계
DNA는 세포핵이라는 좁은 공간 안에 실타래처럼 엉켜 있습니다.
하지만 이 엉킴은 무질서한 것이 아니라, 유전자 발현을 정교하게 조절하는 3차원 아키텍처를 형성합니다.
2026년 3월, 과학자들은 이 구조가 생명의 탄생 순간부터 결정되어 있으며, 이 구조가 무너질 때 질병이 발생한다는 사실을 밝혀냈습니다.
생명이 켜지기 전 DNA의 구조화
오랫동안 생물학자들은 수정란의 DNA가 처음에는 형태 없는 덩어리였다가, 배아가 자신의 유전자를 활성화하는 ‘접합자 게놈 활성화(ZGA)’ 시점에 이르러서야 조직화된다고 생각했습니다.[8]
하지만 Nature Genetics에 발표된 연구는 이 상식을 정면으로 반박하였습니다.
연구진은 ‘Pico-C’라는 초고해상도 3D 매핑 기술을 개발하여 초파리 배아를 분석했습니다.[8]
그 결과, 유전자가 본격적으로 작동하기 훨씬 전부터 이미 정교한 3D 비계(Scaffolding)가 구축되어 있음을 발견했습니다.[8]
개념 정리: 접합자 게놈 활성화(Zygotic Genome Activation, ZGA)란?
수정 직후 배아는 어머니로부터 물려받은 RNA와 단백질에 의존합니다.
그러다 특정 시점이 되면 배아 자신의 게놈이 깨어나 스스로 유전자를 발현하기 시작하는데, 이 결정적인 전환기를 ZGA라고 합니다.
Pico-C 기술은 기존 방식보다 10배나 적은 양의 샘플로도 게놈의 접힘 구조를 포착할 수 있게 해주었습니다.[8]
이 연구를 통해 DNA가 단순한 선형 정보가 아니라, 특정 부위가 고리(Loop)를 형성하여 멀리 떨어진 조절 요소와 만나는 정교한 물리적 네트워크임을 다시 한번 확인하였습니다.[8]
이러한 사전 구조화는 유전자가 필요한 순간에 즉각적으로 반응할 수 있도록 준비하는 ‘분자적 대기 상태’라고 할 수 있습니다.
유전체 구조의 붕괴와 가짜 바이러스 알람
그렇다면 이 정교한 3D 구조가 무너지면 어떤 일이 벌어질까요? Nature Cell Biology에 발표된 동반 연구는 그 치명적인 결과를 보여줍니다.[8]
ETH 취리히의 울리케 쿠타이(Ulrike Kutay) 교수팀은 인간 세포에서 게놈 구조를 지탱하는 ‘분자 닻’인 LBR과 LAP2 단백질을 제거하는 실험을 진행했습니다.[8]
구조적 지지대가 사라지자 게놈의 3D 아키텍처가 붕괴되었고, 놀랍게도 세포는 이를 바이러스가 침입한 상황으로 오인했습니다.[8]
구조가 무너진 DNA 파편들이 세포질로 노출되거나 핵 내의 신호 체계가 교란되면서 선천 면역 시스템이 활성화된 것입니다.[8]
이 ‘가짜 바이러스 알람’은 만성 염증과 세포 사멸을 유도하며, 이는 암이나 자가면역 질환, 노화 관련 퇴행성 질환의 새로운 원인으로 지목되고 있습니다.
즉, 유전자의 ‘내용’뿐만 아니라 그 ‘물리적 배치’를 유지하는 것이 건강을 지키는 핵심이라는 사실이 밝혀진 것입니다.[8]
| 3D 게놈 구성 요소 | 주요 기능 | 구조 붕괴 시 결과 | 출처 |
|---|---|---|---|
| LBR / LAP2 (분자 닻) | DNA를 핵막에 고정하여 구조 안정화 | 게놈 아키텍처 붕괴 및 면역 과잉 반응 | [8] |
| Cohesin (코헤신) | DNA 루프를 형성하여 전사 조절 | 단일 뉴런의 정체성 상실 | [9] |
| TAD (위상학적 관련 도메인) | 특정 유전자군을 물리적으로 격리 | 유전자 조절 네트워크 교란 | [9] |
| ecDNA (염색체 외 DNA) | 종양 내 유전적 다양성 및 가소성 증가 | 암세포의 치료 저항성 및 전이 강화 | [9] |
3D 게놈 구조의 안정성과 질병의 상관관계
최신 연구들은 3D 게놈 구조의 변화가 단순히 발달 과정뿐만 아니라 성숙한 조직의 기능 유지에도 결정적임을 보여줍니다.
예를 들어, 신경계에서는 코헤신(Cohesin) 단백질에 의한 DNA 루프 돌출(Loop extrusion) 과정이 단일 뉴런의 고유한 정체성을 결정하는 데 핵심적인 역할을 합니다.[9]
만약 이 과정에 문제가 생기면 뉴런은 서로 연결되는 데 필요한 올바른 수용체를 만들지 못해 뇌 회로 구성에 실패하게 됩니다.
또한, 노화된 쥐의 뇌를 분석한 연구에서는 이동성 유전인자(Transposon)의 탈메틸화와 함께 TAD 구조의 리모델링이 일어난다는 사실이 확인되었습니다.[9]
이는 나이가 들면서 게놈의 물리적 질서가 서서히 무너지고, 이로 인해 유전자 발현 패턴이 흐트러지면서 인지 기능 저하가 발생할 수 있음을 시사합니다.
따라서 미래의 정밀 의료는 이러한 3D 게놈 구조를 다시 복구하거나 유지하는 전략에 집중하게 될 것입니다.
인공지능과 전산 유전학: 빅데이터로 해독하는 생명의 암호
유전학 데이터가 기하급수적으로 늘어나면서 인간의 직관만으로는 그 의미를 모두 파악하는 것이 불가능했습니다.
하지만 인공지능(AI)이 단순한 보조 도구를 넘어 유전자의 기능을 예측하고 복잡한 생물학적 문제를 해결하는 핵심 파트너로 부상하게 되었습니다.
구글 딥마인드 AlphaGenome: 비부호화 영역의 혁명
단백질 구조 예측 AI인 ‘알파폴드’로 세상을 놀라게 했던 구글 딥마인드 팀이 이번에는 ‘AlphaGenome’을 발표하며 유전학계의 새로운 이정표를 세웠습니다.[10]
AlphaGenome은 최대 100만 염기쌍에 달하는 긴 DNA 서열을 한꺼번에 분석하여, 그 안에 숨겨진 유전적 변이가 생물학적 기능에 어떤 영향을 주는지 예측하는 모델입니다.[10]
우리 DNA의 98%는 단백질을 직접 만들지 않는 ‘비부호화 영역’입니다.
지금까지 대부분의 연구는 2%의 유전자에만 집중해 왔지만, 실제 질병의 90% 이상은 이 신비로운 비부호화 영역의 변이에서 비롯됩니다.[10]
AlphaGenome은 이 거대한 미지의 영역을 해독하여 유전자 발현, 스플라이싱, 단백질 변형 등 5,900개 이상의 유전적 신호를 동시에 예측해 냅니다.[10]
이는 기존의 어떤 모델보다 정밀하며, 특히 유전 질환의 원인을 찾고 새로운 치료 타겟을 발굴하는 데 비약적인 속도 향상을 가져올 것으로 기대됩니다.
단일 세포 데이터의 정밀 복원: scZN 알고리즘
현대 유전학의 총아인 ‘단일 세포 RNA 시퀀싱(scRNA-seq)’은 세포 하나하나의 목소리를 들을 수 있게 해주지만, 기술적 한계로 인해 데이터의 일부가 소실되는 ‘드롭아웃(Dropout)’ 현상이 잦습니다.[11]
2026년 3월 보고된 scZN 프레임워크는 이러한 누락된 데이터를 마법처럼 복구해 내는 기술입니다.
scZN은 ‘사전 가이드 팩터라이제이션(Prior-guided factorization)’ 기술을 사용하여, 가짜 유전자 활성화를 억제하면서도 실제 생물학적 신호만을 정밀하게 살려냅니다.[11]
14가지 기존 알고리즘과의 비교 테스트에서 scZN은 세포의 이질성을 가장 선명하게 복원해 냈으며, 특히 복잡한 질병 모델이나 암 조직 분석에서 세포의 분화 경로나 치료 저항성 세포군을 찾는 데 탁월한 성능을 보였습니다.[11]
| AI / 알고리즘 명칭 | 주요 타겟 및 기능 | 핵심 성과 및 기대 효과 | 출처 |
|---|---|---|---|
| AlphaGenome | 1Mb 범위의 비부호화 DNA 변이 예측 | 유전 질환 진단 정확도 향상 및 신약 타겟 발굴 | [10] |
| scZN | 단일 세포 RNA 시퀀싱 데이터 드롭아웃 복구 | 질병 진행 경로 및 세포 이질성 정밀 분석 | [11] |
| Conservatory | 수백 종의 식물 게놈 비교 분석 도구 | 4억 년 전 보존된 유전적 스위치(CNS) 발굴 | [5] |
| eVAI / VarSome Clinical | 엑솜 데이터 분석 및 변이 우선순위 결정 | 유전적 난청·실명 진단 시간 단축 및 정확도 향상 | [7] |
암 유전학 및 정밀 의료: 세포를 ‘터보차저’로 업그레이드
유전공학은 암 치료의 패러다임을 ‘독성 화학 요법’에서 ‘정밀 면역 요법’으로 바꾸고 있습니다.
전립선암을 저격하는 ‘캐치 본드’ T세포
T세포를 활용한 면역 항암제인 CAR-T 치료제는 혈액암에서 큰 성공을 거두었으나, 전립선암과 같은 고형암에서는 그 효과가 미미했습니다.
고형암은 암세포 주위의 환경이 매우 척박하고, 암세포가 면역 세포의 눈을 피하는 능력이 탁월하기 때문입니다.
UCLA와 스탠포드 대학교 연구팀은 이 문제를 해결하기 위해 T세포에 ‘낚싯바늘’을 달아주는 ‘캐치 본드(Catch Bond) 엔지니어링’ 기술을 개발했습니다.[13]
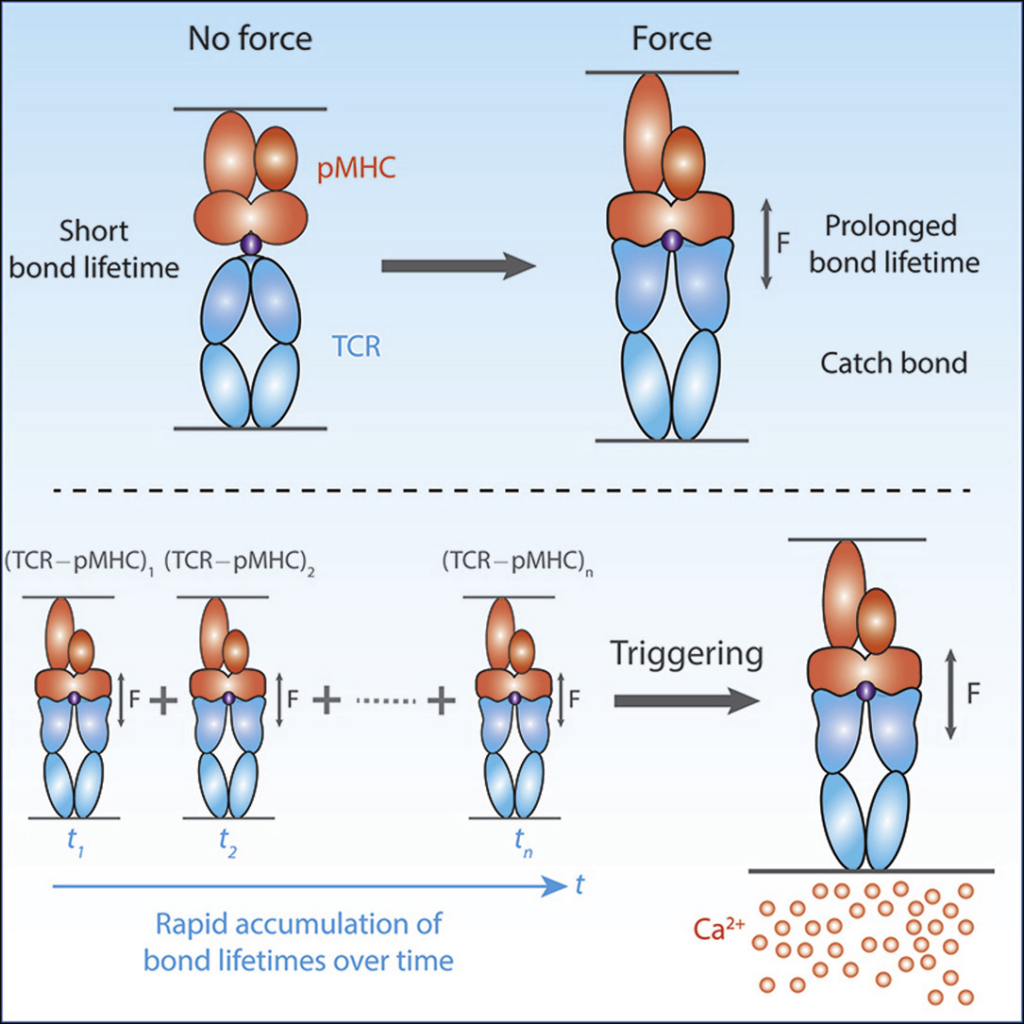
연구진은 T세포 수용체(TCR)의 아미노산 한두 개를 미세하게 수정하여, 암세포와 결합했을 때 물리적인 힘이 가해질수록 결합력이 더욱 강해지도록 설계했습니다.[13]
마치 낚싯바늘이 한 번 걸리면 잡아당길수록 더 깊게 박히는 것과 같은 원리입니다.
이렇게 ‘터보차저’가 장착된 T세포는 전립선암의 특이 단백질인 PAP를 매우 정밀하게 인식하며, 암세포의 방어막을 뚫고 끝까지 추적하여 사멸시킵니다.[13]
골육종의 희망: OSM CAR-T 세포 치료제
어린이와 청소년에게 주로 발생하는 치명적인 뼈암인 골육종은 지난 40년간 생존율 향상이 거의 없었던 질병입니다.
케이스 웨스턴 리저브 대학교 연구팀은 골육종 세포 표면에 흔히 나타나는 온코스타틴 M(OSM) 수용체를 공략하는 새로운 CAR-T 치료제를 개발했습니다.[14]
OSM CAR-T 치료제는 쥐 모델 실험에서 골육종 종양을 효과적으로 파괴했을 뿐만 아니라, 폐 등 다른 장기로 전이된 암세포까지 추적하여 제거하는 성능을 보였습니다.[14]
기존 항암제보다 부작용이 훨씬 적으면서도 강력한 항종양 효과를 발휘한다는 점이 고무적입니다. 연구팀은 향후 2년 내에 임상 시험에 진입할 수 있을 것으로 내다보고 있습니다.[14]
액체 생검과 AI 기반 암 진단의 최전선
암 진단 기술 또한 유전학의 발전과 궤를 같이하고 있다. 최근에는 혈액 속에 떠다니는 암세포 유래 DNA(cfDNA)를 분석하는 ‘액체 생검’ 기술이 암의 조기 진단과 치료 모니터링에 필수적인 도구가 되었습니다.[3]
여기에 AI 기반의 통합 멀티오믹스 분석이 더해지면서 진단의 정확도는 더욱 높아지고 있습니다.[15]
예를 들어, 췌장암 치료를 위해 나노입자를 활용한 표적 약물 전달 시스템이 연구되고 있으며, Kupffer 세포를 타겟팅하여 방사선 유발 간 손상을 완화하는 리포좀 기술도 개발되었습니다.[16]
또한, 포르말린 고정 파라핀 보관(FFPE) 과정에서 발생하는 아티팩트를 AI로 식별하여 데이터의 신뢰성을 높이는 모델도 등장했습니다.[9]
이러한 기술들은 암 치료의 정밀도를 극대화하여 환자 개개인에게 최적화된 ‘맞춤형 암 치료’를 실현하고 있습니다.
| 암 종류 | 타겟 분자 / 기술 | 연구 성과 및 특징 | 출처 |
|---|---|---|---|
| 전립선암 | PAP (캐치 본드 TCR) | 결합력 강화를 통한 고형암 침투 및 사멸 능력 향상 | [13] |
| 골육종 (뼈암) | Oncostatin M (OSM) 수용체 | 전이된 종양 세포까지 효과적으로 제거하는 CAR-T 치료제 | [14] |
| 췌장암 | TGN46 (바이러스 수용체) | 온콜리틱 바이러스(H-1PV)의 감염 효율을 결정하는 핵심 인자 규명 | [17] |
| 식도암 | HSP90AA1 (PRMT5 매개) | 아르기닌 메틸화를 통한 암 진행 및 전이 메커니즘 차단 타겟 | [18] |
| 교모세포종 | ecDNA (염색체 외 DNA) | 암세포의 유전적 가소성 및 약물 저항성 기전 분석 | [9] |
신경 유전학: 뇌의 신비를 푸는 유전적 지도
인간의 뇌는 유전체 연구에서 가장 까다로운 영역 중 하나입니다.
하지만, 과학자들은 단일 세포 수준의 정밀한 분석을 통해 뇌 질환의 유전적 뿌리를 캐는 데 성공했습니다.
뇌 질환의 세포별 유전적 위험 분석
과거에는 특정 유전자 변이가 질병을 일으킨다는 사실만 알았을 뿐, 그 유전자가 뇌의 어떤 세포에서 문제를 일으키는지는 알기 어려웠습니다.
뉴욕 게놈 센터와 다국적 연구팀은 단일 핵 수준의 발현 양적 형질 유전자좌(single-nucleus eQTL) 분석을 통해 뇌 질환의 유전적 위험을 실제 뇌 기능과 연결하는 지도를 완성했습니다.[9]
이들은 수만 개의 뇌 세포 데이터를 메타 분석하여 조현병, 자폐증, 알츠하이머병 등의 위험 변이가 뉴런이나 성상세포, 미세아교세포에서 각각 어떻게 유전자 발현을 변화시키는지 규명했습니다.[9]
예를 들어, 특정 유전자 변이는 오직 신경 교세포(Glia)에서만 스플라이싱 패턴을 바꾸어 염증을 유발한다는 사실이 밝혀진 것입니다.
이는 뇌 질환 치료를 위해 단순히 유전자를 타겟팅하는 것이 아니라, 특정 ‘세포 타입’을 조준해야 한다는 사실을 시사합니다.
노화하는 뇌의 게놈 구조 변화와 퇴행성 질환
노화는 뇌의 게놈에도 지울 수 없는 흔적을 남깁니다.
쥐의 실질(Substantia nigra) 부위를 단일 핵 멀티오믹스로 분석한 결과, 파킨슨병과 관련된 유전적 변화가 노화 과정에서 어떻게 누적되는지가 밝혀졌습니다.[9]
특히 노화된 뇌 세포에서는 이동성 유전인자(Transposon) 주변의 메틸기가 사라지면서(탈메틸화), 억제되어 있던 유해 유전자들이 다시 살아나 염증을 일으키고 뇌 세포를 손상시킨다는 사실이 확인되었습니다.[9]
또한, 3D 게놈 구조의 기본 단위인 TAD(Topologically Associating Domains)의 리모델링이 노화와 밀접하게 관련되어 있다는 점도 주목할 만합니다.[9]
이는 뇌의 노화가 단순히 에너지가 고갈되는 과정이 아니라, 유전체를 지탱하는 물리적 질서가 붕괴되는 과정임을 보여줍니다.
참고자료
- This CRISPR breakthrough turns genes on without cutting DNA – ScienceDaily, https://www.sciencedaily.com/releases/2026/01/260104202813.htm
- Mammalian genome writing: Unlocking new length scales for genome engineering, https://pubmed.ncbi.nlm.nih.gov/41576918/
- Life Science and Biotech Trends for 2026 – AZoLifeSciences, https://www.azolifesciences.com/article/Life-Science-and-Biotech-Trends-for-2026.aspx
- Precision Genome Engineering: From Basic Mechanisms to Application – Keystone Symposia on Molecular and Cellular Biology, https://www.keystonesymposia.org/conferences/conference-listing/meeting/l12026
- Scientists discover ancient DNA “switches” hidden in plants for 400 …, https://www.sciencedaily.com/releases/2026/03/260313062533.htm
- Boosting crops’ natural capabilities could help feed a warming world – PNAS, https://www.pnas.org/doi/10.1073/pnas.2607080123
- Genes, Volume 17, Issue 3 (March 2026) – 95 articles – MDPI, https://www.mdpi.com/2073-4425/17/3
- Stunning 3D maps reveal DNA is structured before life “switches on …, https://www.sciencedaily.com/releases/2026/02/260227061824.htm
- Publications – New York Genome Center – Genomic Research, https://www.nygenome.org/publications/
- Genomics: AlphaGenome predicts the impact of DNA variations (Nature), https://www.natureasia.com/en/info/press-releases/detail/9222
- Prior-guided factorization for reliable imputation of scRNA-seq data | PLOS Computational Biology – Research journals, https://journals.plos.org/ploscompbiol/article?id=10.1371/journal.pcbi.1014051
- Tricorder Tech: Protein Sequencing Advance Offers New Insights …, https://astrobiology.com/2026/03/tricorder-tech-protein-sequencing-advance-offers-new-insights-into-lifes-foundations.html
- Scientists “turbocharge” immune cells to attack prostate cancer – UCLA Health, https://www.uclahealth.org/news/release/scientists-turbocharge-immune-cells-attack-prostate-cancer
- Researchers develop promising new therapy for most common form of bone cancer in children and young adults | EurekAlert!, https://www.eurekalert.org/news-releases/1119954
- New genomic and proteomic biomarker discovery in cancer: revolutionizing diagnosis and prognostication – PMC, https://pmc.ncbi.nlm.nih.gov/articles/PMC12918557/
- Int. J. Mol. Sci., Volume 27, Issue 5 (March-1 2026) – 432 articles – MDPI, https://www.mdpi.com/1422-0067/27/5
- A genome-wide CRISPR-Cas9 screen identifies TGN46 as a host determinant for H-1PV susceptibility in pancreatic adenocarcinoma | bioRxiv, https://www.biorxiv.org/content/10.64898/2026.03.06.710102v2
- TITLE PAGE PRMT5-Mediated Arginine Methylation of HSP90AA1 Drives Esophageal Squamous Cell Carcinoma Progression Tangbing Chen1 – bioRxiv, https://www.biorxiv.org/content/10.64898/2026.03.09.710340v1.full.pdf
- Cognitive Neuroscience Society: Home, https://www.cogneurosociety.org/
- Positive Selection Targeted Primate Genes that Encode Transposable Element Repressors | Genome Biology and Evolution | Oxford Academic, https://academic.oup.com/gbe/article-abstract/doi/10.1093/gbe/evag059/8507158
- Scientists confirm the discovery of an exceptionally large African python during a certified field expedition – T G G News, https://www.thegrapeandgrain.com.au/scientists-confirm-the-discovery-of-an-exceptionally-large-african-python-during-a-certified-field-expedition/
- GigaScience | Oxford Academic, https://academic.oup.com/gigascience