오늘날 현대인들이 마주하는 가장 큰 공포 중 하나는 아마도 ‘암’이라는 질병일 것입니다. 기술이 아무리 발전해도 암은 여전히 정복하기 힘든 성벽처럼 느껴지곤 하는데요.
그런데 만약, 암세포가 단순히 돌연변이를 일으키는 수준을 넘어 우리가 투여하는 항암제를 실시간으로 ‘학습’하고 그에 맞춰 자신의 유전적 회로를 재배선하고 있다면 어떨까요? [1]
2026년 4월, 세계 최고의 과학 저널에서는 우리가 미처 몰랐던 면역 체계의 신비로운 이면을 파헤치는 논문들이 쏟아져 나왔습니다.
진화의 역설: 1만 년의 기록이 들려주는 생존의 대가
인류의 면역 시스템은 하루아침에 뚝딱 만들어진 것이 아닙니다.
지난 수만 년 동안 끊임없는 바이러스와 세균의 공격 속에서, 오직 살아남은 자들의 유전자만이 오늘날 우리의 몸속에 흐르고 있습니다. [3, 7]
2026년 4월 Nature에 발표된 한 대규모 고대 DNA 연구는 이 ‘생존의 유산’이 현대인에게 어떤 영향을 미치고 있는지 극명하게 보여줍니다. [3]
10,000년 전 조상이 남긴 유전적 갑옷과 그 부작용
하버드 대학교를 비롯한 국제 공동 연구진은 서유라시아 지역에서 발굴된 약 16,000구의 고대 인류 유골에서 추출한 DNA를 분석했습니다. [3, 7]
이들은 수렵 채집 생활에서 농경 사회로 전환되던 시기, 즉 인구가 밀집되고 가축과의 접촉이 늘어나면서 전염병의 위협이 급증했던 때에 어떤 유전자들이 선택되었는지 추적했습니다. [2, 7]
연구 결과, 결핵(TB)이나 독감, 장내 감염증과 같은 치명적인 질병으로부터 신체를 보호하기 위해 특정 면역 유전자들이 급격히 확산되었다는 사실이 밝혀졌습니다. [2]
하지만 놀라운 반전은 여기서 시작됩니다. 과거에 감염병으로부터 우리를 지켜주었던 이 강력한 면역 반응 유전자들이, 오늘날 위생적인 환경에서는 오히려 자기 자신을 공격하는 자가면역 질환의 강력한 위험 요인이 되고 있었기 때문입니다. [2]
| 선택된 유전자 및 변이 | 과거의 생존 이점 (감염병 저항) | 현대의 질병 위험 (자가면역/염증) |
|---|---|---|
| FUT6 | 장내 감염 및 기생충 방어 | 염증성 장질환(IBD) 위험 증가 |
| ASAP1 | 결핵(TB) 균 확산 억제 | 자가면역성 갑상선 질환 위험 상승 |
| LYZ (리소자임) | 세균 벽 분해 및 항균 작용 | 만성 염증 지표 상승 및 조직 손상 |
| TNFRSF1A | 감염병에 대한 빠른 면역 반응 | 다발성 경화증(MS) 감수성 증가 |
이 데이터는 인류의 진화가 완벽함을 향한 여정이 아니라, 주어진 환경에서 살아남기 위한 치열한 ‘거래(Trade-off)’의 연속이었음을 시사합니다. [2]
전염병으로 죽지 않기 위해 면역의 감도를 극도로 높여놓았더니, 이제는 전염병이 사라진 자리에서 그 높은 감도가 아군을 쏘는 오발 사고를 내고 있는 셈입니다. [2]
암세포의 영리한 ‘학습’ 모델: AP-1 단백질의 비밀
암 치료가 왜 그렇게 힘들까요? 가장 큰 원인은 암이 약물에 대해 ‘내성’을 갖기 때문입니다. [1]
지금까지 우리는 암세포가 무작위적인 돌연변이를 일으키다가 우연히 약물에 안 죽는 놈이 살아남는 것이라고 생각했습니다. [1]
하지만 2026년 4월 15일, Nature의 표지를 장식한 뉴욕 대학교(NYU) 랑곤 헬스 연구팀의 논문은 암세포가 마치 인공지능처럼 ‘학습’을 통해 변신한다는 새로운 모델을 제시했습니다. [1]
진화 알고리즘처럼 작동하는 암세포
이타이 야나이(Itai Yanai) 박사팀은 암세포가 환경적 스트레스(예: 항암제 투여)를 받았을 때 빠르게 활성화되는 AP-1이라는 단백질 가족에 주목했습니다. [1]
이 단백질들은 세포 내의 유전적 회로를 실시간으로 재배선(Rewiring)하는 지휘자 역할을 합니다. [1]
- 탐색 단계: 항암제가 들어오면 암세포는 생존을 위해 다양한 유전자 발현 패턴을 시도합니다. 이를 ‘전사적 가소성(Transcriptional Plasticity)’이라고 부릅니다. [1]
- 학습 및 최적화: AP-1은 수많은 유전자 조합 중 스트레스를 가장 잘 견뎌내는 패턴을 찾아냅니다. 마치 강화 학습 알고리즘이 정답을 찾아가는 과정과 비슷합니다. [1]
- 고정 및 전수: 생존에 유리한 상태가 발견되면, 암세포는 이 상태를 세포 내에 고정하고 다음 세대 세포들에게 그대로 물려줍니다. [1]
이것은 암세포가 단순히 운이 좋아 살아남는 것이 아니라, 적극적으로 생존 방법을 ‘학습’하고 있다는 것을 의미합니다. [1]
연구팀은 이제 암세포의 특정 상태를 공격하는 기존 방식에서 벗어나, 암세포의 이러한 ‘적응 능력’ 자체를 차단하는 항적응제(Anti-adaptation agents) 개발이 필요하다고 강조합니다. [1]
[개념 쏙쏙] 전사적 가소성(Transcriptional Plasticity)이란?
DNA 서열 자체는 바뀌지 않으면서, 상황에 따라 유전자를 켜고 끄는 방식(발현 패턴)을 유연하게 바꾸는 능력을 말합니다. 암세포는 이 능력을 이용해 카멜레온처럼 모습을 바꿉니다. [1]
[개념 쏙속] AP-1(Activator Protein-1) Family란?
AP-1(Activator Protein-1) 단백질군은 세포 내 신호 전달의 종착지에서 유전자의 발현을 조절하는 가장 대표적인 전사 인자(Transcription Factor) 복합체입니다.
세포의 증식, 분화, 사멸, 그리고 스트레스 반응에 이르기까지 광범위한 생물학적 프로세스를 제어합니다.
암세포의 이중성: AP-1은 전통적으로 ‘Oncoprotein(암 유발 단백질)’으로 간주되었으나, 최근에는 특정 조직이나 환경에서 종양 억제(Tumor suppression) 기능을 수행할 수 있다는 가설이 힘을 얻고 있습니다.
구조적 특징: AP-1은 단일 단백질이 아니라, bZIP(basic leucine zipper) 도메인을 가진 단백질들이 결합한 이량체(Dimer) 형태입니다. 주요 구성 성분은 Jun 패밀리(c-Jun, JunB, JunD)와 Fos 패밀리(c-Fos, FosB, Fra-1, Fra-2)입니다.
결합 기전: 이들은 DNA의 특정 염기서열인 TRE(TPA-responsive element, 5′-TGAG/CTCA-3′) 또는 CRE(cAMP-responsive element)에 결합하여 하위 유전자의 전사를 활성화하거나 억제합니다.
이량체 형성의 규칙: Jun 패밀리는 스스로 결합하는 동종이량체(Homodimer)와 Fos와 결합하는 이종이량체(Heterodimer)를 모두 형성할 수 있습니다.
췌장암의 철벽 수비를 무너뜨리는 ‘T세포 리프로그래밍’
췌장암은 면역 항암제가 잘 듣지 않기로 유명한 지독한 암입니다. [4]
췌장암 세포 주변에는 마치 철벽처럼 면역 세포의 접근을 막는 환경이 조성되어 있기 때문인데요. [4]
2026년 4월 10일 Immunity 저널에 발표된 오리건 건강과학대학교(OHSU)의 연구는 이 철벽을 뚫을 수 있는 새로운 전략을 공개했습니다. [4]
조절 T세포(Treg): 배신자를 우리 편으로!
췌장암 내부에는 조절 T세포(Tregs)라고 불리는 세포들이 가득합니다. [4]
원래 이들은 우리 몸에서 면역 반응이 너무 과해지지 않도록 진정시키는 ‘평화유지군’ 역할을 하지만, 암세포는 이들을 매수하여 암을 공격하려는 킬러 T세포(CD8+ T세포)를 잠재우는 용도로 사용합니다. [4, 8]
연구진은 CD40 항진제(Agonistic CD40)라는 약물을 사용해 놀라운 실험을 진행했습니다. [4]
이 약물은 단순히 면역을 활성화하는 것을 넘어, 암세포에 매수되었던 조절 T세포의 성질을 완전히 바꾸어버렸습니다. [4]
억제만 하던 세포들이 갑자기 암세포를 공격하도록 돕는 지원군으로 ‘리프로그래밍’된 것입니다. [4]
| 치료 전략 | 주요 메커니즘 | 기대 효과 |
|---|---|---|
| 체크포인트 억제제 | T세포의 브레이크를 제거 | 일반적인 암에서 효과적이나 췌장암에선 한계 |
| CD40 항진제 | 조절 T세포(Treg)를 공격군으로 전환 | 췌장암의 면역 억제 환경 타파 [4] |
| 병용 요법 (KRAS 억제제+) | 암세포 직접 공격 + 면역 환경 개선 | 시너지 효과를 통한 완치율 상승 [4] |
이 연구는 환자 개인의 종양 특성에 맞춰, Tregs가 많은 종양에는 이 리프로그래밍 전략을 사용하는 정밀 의료의 시대를 앞당기고 있습니다. [4]
[개념 쏙쏙] Agonist / Antagonist
1. Agonist (효능제/항진제)
수용체에 결합하여 그 수용체를 활성화하고 생물학적 반응을 유도하는 물질입니다. 열쇠 구멍(수용체)에 맞는 열쇠(Agonist)가 들어가 문을 여는 것과 같습니다.
- Full Agonist (완전 효능제): 수용체에 결합하여 해당 수용체가 낼 수 있는 최대 반응을 이끌어냅니다.
- Partial Agonist (부분 효능제): 수용체에 결합은 하지만, 최대치보다 낮은 수준의 반응만을 유도합니다.
2. Antagonist (길항제/차단제)
수용체에 결합은 하지만 자체적으로는 수용체를 활성화하지 않으며, 오히려 Agonist가 결합하는 것을 방해하는 물질입니다.
열쇠 구멍에 들어가 박혀서 진짜 열쇠가 들어오지 못하게 막는 ‘부러진 열쇠’나 ‘껌’과 같습니다.
Non-competitive Antagonist (비경쟁적 길항제): Agonist와 다른 부위에 결합하여 수용체의 구조를 변형시킴으로써 Agonist가 제 기능을 못 하게 합니다.
Competitive Antagonist (경쟁적 길항제): Agonist와 같은 결합 부위를 두고 서로 경쟁합니다.
세포 공학의 정점: 염기 편집(Base Editing)으로 만드는 슈퍼 NK 세포
최근 면역학의 화두는 단순히 면역을 돕는 것이 아니라, 면역 세포를 아예 ‘재설계’하는 것입니다. [9]
2026년 4월 15일 Cancer Research에 발표된 연구는 자연살해(NK) 세포의 기능을 극대화하기 위해 유전자 가위 기술 중에서도 가장 정교하다는 ‘염기 편집’ 기술을 도입했습니다. [9]
TIGIT: NK 세포의 눈을 가리는 단백질
암세포는 살아남기 위해 NK 세포의 표면에 있는 TIGIT이라는 수용체를 자극합니다. [9]
TIGIT이 자극받으면 NK 세포는 암세포를 보고도 “아, 아군이구나” 하고 지나치게 됩니다. [9] 연구진은 이 TIGIT 유전자를 염기 편집 기술로 살짝 바꾸어버렸습니다. [9]
그 결과는 놀라웠습니다. 단순히 TIGIT이 사라진 것을 넘어, 암세포가 보낸 “공격 중단” 신호가 NK 세포 내부에서 오히려 “공격 개시” 신호(CD226 활성화)로 바뀌어 전달되는 현상이 관찰되었습니다. [9]
마치 적군이 보낸 항복 권유 메시지를 보고 아군이 더욱 전의를 불태우게 만든 것과 같습니다. [9]
특히 이 방식은 DNA 두 가닥을 모두 자르지 않는 염기 편집 기술을 사용했기 때문에, 유전자 변형 시 발생할 수 있는 오프타깃(Off-target) 부작용이 거의 없어 안전성까지 확보했습니다. [9]
[개념 쏙쏙] TIGIT(T-cell immunoreceptor with Ig and ITIM domains)
NK 세포(Natural Killer cell) 표면에 발현되는 TIGIT(T-cell immunoreceptor with Ig and ITIM domains)는 면역 반응을 억제하는 대표적인 면역 관문 수용체(Immune Checkpoint Receptor)입니다.
암세포나 바이러스 감염 세포가 면역 공격을 피하기 위해 사용하는 핵심 방어 기전 중 하나입니다.
- 억제성 수용체: TIGIT은 NK 세포의 활성을 억제하여 표적 세포를 공격하지 못하게 만드는 ‘브레이크’ 역할을 합니다.
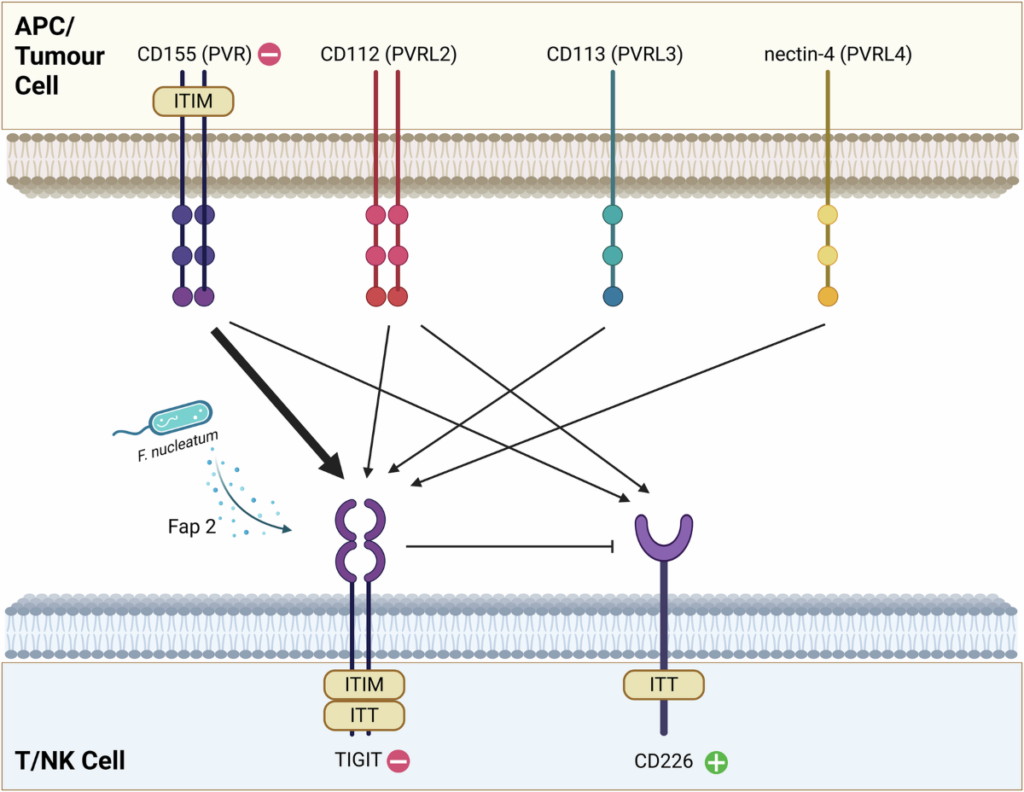
- 리간드와의 결합: TIGIT은 주로 표적 세포(암세포 등) 표면에 있는 PVR(CD155) 또는 PVRL2(CD112) 단백질과 결합합니다.
- 동작 원리 (신호 전달): TIGIT의 세포질 내 도메인에는 ITIM 및 ITT-like 모티프가 있습니다. PVR과 결합하면 이 부위가 인산화되면서 억제성 인자(SHIP1 등)를 불러모으고, NK 세포의 살상 신호(세포독성 과립 방출 등)를 차단합니다.
- 경쟁적 저해: TIGIT은 활성화 수용체인 DNAM-1(CD226)과 동일한 리간드(PVR)를 공유합니다. 하지만 TIGIT은 DNAM-1보다 PVR에 대한 결합 친화도(Affinity)가 훨씬 높습니다. 따라서 PVR을 선점함으로써 DNAM-1이 보내는 ‘공격 신호’를 원천 봉쇄합니다.
자가면역 질환 치료의 혁명: ALLO-329와 이중 타격 전략
암 치료에서 큰 성공을 거둔 CAR-T 세포 치료제가 이제 자가면역 질환인 루푸스(SLE)를 정복하러 나섰습니다. [10, 11]
2026년 4월 15일 Nature Communications에는 올로진 테라퓨틱스(Allogene Therapeutics)가 개발한 차세대 CAR-T 치료제인 ALLO-329의 연구 데이터가 공개되었습니다. [11]
B세포와 활성 T세포를 동시에 잡는다
루푸스는 우리 몸의 B세포가 자기 자신을 공격하는 항체를 만들어내기 때문에 발생합니다. [11] 하지만 단순히 B세포만 제거해서는 효과가 부족할 때가 많습니다. [10]
ALLO-329는 이 문제를 해결하기 위해 CD19(B세포 타깃)와 CD70(활성 T세포 타깃)을 동시에 공격하는 이중 CAR-T 기술을 적용했습니다. [10, 12]
- CD19 타격: 자가 항체를 만드는 주범인 B세포를 빠르게 제거합니다. [11]
- CD70 타격: 염증을 악화시키는 ‘미친 T세포’들을 골라내어 처단합니다. [11]
- Dagger® 기술: 외부에서 들어온 CAR-T 세포가 환자의 몸속에서 거부당하지 않고 오랫동안 살아남아 활동할 수 있게 해주는 보호막 기술입니다. [11, 12]
현재 루푸스뿐만 아니라 경피증, 염증성 근염 환자들을 대상으로 임상 1상 시험이 진행 중이며, 2026년 6월이면 첫 번째 투여 결과가 나올 예정이라고 하니 전 세계 자가면역 질환 환자들에게 큰 희망이 될 것으로 보입니다. [13, 14]
노화의 정체: 내 몸속의 ‘좀비 세포’를 찾아라!
우리가 늙는다는 것은 단순히 시간이 흐르는 것 이상의 생물학적 변화를 수반합니다. [15, 16]
2026년 4월 16일, UCLA 연구팀은 우리가 흔히 겪는 지방간과 전신 노화의 주범이 사실은 우리 몸속의 ‘노화된 면역 세포’였다는 사실을 밝혀냈습니다. [15]
간 질환을 일으키는 범인, p21-TREM2 대식세포
연구팀은 나이가 들면서 간 속에 p21과 TREM2라는 단백질을 동시에 가진 특이한 대식세포들이 쌓인다는 것을 발견했습니다. [15]
이 세포들은 면역 세포 본연의 임무인 ‘청소’는 하지 않으면서, 주변 세포들에게 염증 신호를 마구 뿌려대는 ‘좀비’ 같은 존재들입니다. [15]
놀랍게도 쥐 실험에서 이 좀비 세포들만 선택적으로 제거했더니, 지방간 증상이 개선되고 간 조직이 다시 젊어지는 현상이 나타났습니다. [15]
이는 노화 자체가 하나의 질병이며, 특정 면역 세포만 잘 다스려도 노화 속도를 늦출 수 있다는 ‘거로사이언스(Geroscience)’ 가설을 뒷받침하는 강력한 증거입니다. [15]
혈액 줄기세포의 에너지 도둑, MLKL
노화의 또 다른 비밀은 우리 몸의 모든 혈액을 만들어내는 ‘조혈 줄기세포(HSC)’에 숨어 있었습니다. [16]
도쿄 대학교 연구팀은 2026년 4월 Nature Communications를 통해, 원래 세포를 죽이는 것으로 알려졌던 MLKL 단백질이 조혈 줄기세포에서는 죽음 대신 ‘에너지 고갈’을 유발한다는 사실을 발표했습니다. [16]
MLKL은 줄기세포의 에너지 공장인 미토콘드리아를 망가뜨려 세포를 무력하게 만듭니다. [16]
이 메커니즘을 차단하면 나이가 들어도 쌩쌩한 면역 시스템을 유지할 수 있는 길이 열릴지도 모릅니다. [16]
백신과 기억의 과학
마지막으로 우리가 백신을 맞으면 왜 그 기억이 오래가는지, 그리고 왜 코로나19나 독감 백신은 자주 맞아야 하는지에 대한 의문을 풀어보겠습니다. [6]
세계적인 면역학자 셰인 크로티(Shane Crotty) 박사는 2026년 4월 Immunity 리뷰를 통해 ‘면역 기억’의 놀라운 지속성을 설명했습니다. [6]
림프절: 면역 세포들의 훈련소
우리 몸의 B세포들은 백신을 맞으면 림프절 안에 있는 ‘생성 중심(Germinal Center)’이라는 곳으로 들어갑니다. [6]
이곳은 일종의 부트캠프로, B세포들은 여기서 바이러스를 더 잘 잡기 위해 자신의 항체를 계속해서 업그레이드합니다. [6]
훈련을 마친 ‘기억 B세포’들은 수십 년 동안 우리 몸을 지킵니다. [6]
실제로 어릴 때 천연두 백신을 맞은 사람들을 조사해 보니, 60년이 지난 후에도 혈액 속에 기억 B세포가 살아있었다고 합니다. [6]
- 지속성: 백신에 의해 생성된 면역 기억은 생각보다 훨씬 오래갑니다. [6]
- 도전: 문제는 바이러스가 너무 빨리 변한다는 것입니다. 백신의 기억이 사라진 것이 아니라, 적군이 옷을 갈아입고 나타나서 못 알아보는 것입니다. [6]
- 미래: 과학자들은 이제 항체 수치만 높이는 것이 아니라, 적군이 어떤 옷으로 갈아입어도 알아볼 수 있도록 B세포의 ‘훈련 강도’를 높이는 새로운 백신 기술을 개발 중입니다. [6]
참고자료
- How Do Cancer Cells ‘Learn’ to Resist Treatment? | NYU Langone …, https://nyulangone.org/news/how-do-cancer-cells-learn-resist-treatment
- Ancient DNA reveals that natural selection has upregulated the …, https://www.biorxiv.org/content/10.64898/2026.04.14.718409v1
- Groundbreaking Ancient DNA Study Uncovers Accelerated Natural Selection in Recent Human Evolution – Bioengineer.org, https://bioengineer.org/groundbreaking-ancient-dna-study-uncovers-accelerated-natural-selection-in-recent-human-evolution/
- OHSU research reveals how pancreatic cancer blocks …, https://news.ohsu.edu/2026/04/10/ohsu-research-reveals-how-pancreatic-cancer-blocks-immunotherapy
- The Ancient Weapons Active in Your Immune System Today | Quanta Magazine, https://www.quantamagazine.org/the-ancient-weapons-active-in-your-immune-system-today-20260415/
- We’re taking a closer look at immune ‘memory’ – lji.org, https://www.lji.org/news-events/news/post/crotty-vaccine-immune-memory/
- Massive Ancient-DNA Study Reveals Natural Selection Has Accelerated in Recent Human Evolution | Harvard Medical School, https://hms.harvard.edu/news/massive-ancient-dna-study-reveals-natural-selection-has-accelerated-recent-human-evolution
- Day of Immunology 2026 | Regulatory T Cells: Guardians of Immune… – IUIS Immunohub, https://immunohub.iuis.org/iuis/2026/webinars/4193475
- Base Editing of TIGIT Reprograms CD155 Signaling in Natural Killer Cells to Enhance Cancer Immunotherapy Efficacy – AACR Journals, https://aacrjournals.org/cancerres/article/86/8/1956/782640/Base-Editing-of-TIGIT-Reprograms-CD155-Signaling
- Allogene Therapeutics Announces Nature Communications …, https://www.biospace.com/press-releases/allogene-therapeutics-announces-nature-communications-publication-highlighting-pre-clinical-data-for-allo-329-a-next-generation-dual-targeted-cd19-cd70-allogeneic-car-t-for-autoimmune-diseases
- Allogene Therapeutics Announces Nature Communications Publication Highlighting Pre-Clinical Data for ALLO-329, a Next Generation Dual-Targeted CD19/CD70 Allogeneic CAR T for Autoimmune Diseases, https://ir.allogene.com/news-releases/news-release-details/allogene-therapeutics-announces-nature-communications
- Allogene Therapeutics Announces Nature Communications Publication Highlighting Pre-Clinical Data for ALLO-329, a Next Generation Dual-Targeted CD19/CD70 Allogeneic CAR T for Autoimmune Diseases | Markets Insider, https://markets.businessinsider.com/news/stocks/allogene-therapeutics-announces-nature-communications-publication-highlighting-pre-clinical-data-for-allo-329-a-next-generation-dual-targeted-cd19-cd70-allogeneic-car-t-for-autoimmune-diseases-1036024641
- Allogene publishes preclinical data for dual-targeted autoimmune CAR T – StreetInsider, https://www.streetinsider.com/Corporate+News/Allogene+publishes+preclinical+data+for+dual-targeted+autoimmune+CAR+T/26315543.html
- Allogene Therapeutics Announces The Publication Of Pre-Clinical Data For ALLO-329, An Investigational Allogeneic CAR T Product Developed Specifically For Autoimmune Diseases, In The Journal ‘Nature Communications’ – Sahm Stock Trading, https://www.sahmcapital.com/news/content/allogene-therapeutics-announces-the-publication-of-pre-clinical-data-for-allo-329-an-investigational-allogeneic-car-t-product-developed-specifically-for-autoimmune-diseases-in-the-journal-nature-communications-2026-04-15
- Scientists remove “zombie” cells and reverse liver damage in mice | ScienceDaily, https://www.sciencedaily.com/releases/2026/04/260416071947.htm
- A “death” protein may be the key to slowing aging at its source – ScienceDaily, https://www.sciencedaily.com/releases/2026/04/260416071951.htm
- PROGRAM – immunology2026 – The American Association of Immunologists, https://immunology2026.aai.org/wp-content/uploads/2026/03/IMMUNOLOGY2026%E2%84%A2_Program_Preview_Web.pdf
- MMBIO Honored Graduate: How Faith and Persistence Guided Emily Shakespear’s Academic Journey – BYU Life Sciences, https://lifesciences.byu.edu/mmbio-honored-graduate-how-faith-and-persistence-guided-emily-shakespears-academic-journey
- Mount Sinai Researchers Highlight Advances in Cancer Science at 2026 AACR Annual Meeting in San Diego, https://www.mountsinai.org/about/newsroom/2026/mount-sinai-researchers-highlight-advances-in-cancer-science-at-2026-aacr-annual-meeting-in-san-diego
- Home – IMMUNOLOGY2026™ – The American Association of Immunologists, https://immunology2026.aai.org/
- AACR Annual Meeting 2026, https://www.aacr.org/meeting/aacr-annual-meeting-2026/