우리는 흔히 면역력을 ‘감기에 걸리지 않는 힘’ 정도로만 생각하곤 합니다. 하지만 2026년 3월 과학 저널들이 쏟아낸 논문들은 우리의 면역 체계가 생각보다 훨씬 더 드라마틱하고, 정교한 전략을 구사하고 있다는 사실을 보여주고 있습니다.
암 정복의 새로운 열쇠
우리 몸의 대식세포(Macrophage)는 원래 침입자를 잡아먹는 든든한 아군입니다.
하지만 암세포 주변에만 가면 이 대식세포들이 암세포의 성장을 돕는 ‘배신자’로 변하곤 하죠.
2026년 3월 Nature Immunology에 발표된 Li 등의 연구는 이 배신자 대식세포를 다시 정의로운 전사로 되돌릴 혁신적인 방법을 찾아냈습니다.[1]
대식세포의 배신을 멈추게 하는 물리적 장벽의 비밀
이 연구의 핵심은 ‘Notch 신호‘라는 것입니다.
원래 대식세포가 죽어가는 세포를 처리하는 ‘세포 포식(Efferocytosis)’ 과정 중에는 우리 몸의 과도한 염증을 막기 위해 Notch 신호가 차단됩니다.
연구팀은 대식세포 표면에서 Rubcn–VPS34 복합체가 활성화되면서 ‘인테그린 장벽’이라는 물리적인 담벼락을 쌓는다는 사실을 발견했습니다.[1]
이 담벼락은 Notch 수용체가 암세포의 신호를 받지 못하도록 물리적으로 밀어내는 역할을 합니다.
놀라운 점은 Phospholipase D(PLD) 효소를 억제하거나 Rubicon 유전자를 조절하면 이 장벽이 무너지면서 Notch 신호가 다시 살아난다는 것입니다.[1]
이렇게 성격이 바뀐 대식세포는 종양 내부로 ‘킬러 T 세포’인 CD8+ T 세포를 대거 불러들여 암세포를 초토화합니다.[1]
이는 단순한 약물 투여를 넘어, 면역 세포의 ‘물리적 구조’를 바꿔 치료 효율을 높이는 3차원적 치료 전략의 시대를 열었다고 평가받습니다.
| 조절 인자 | 면역학적 기능 | 항암 전략 방향 |
|---|---|---|
| Rubicon-VPS34 복합체 | 대식세포 표면의 인테그린 장벽 형성 주도 [1] | 해당 복합체 억제를 통해 Notch 신호 복구 |
| Phospholipase D (PLD) | 인테그린 활성화를 통한 Notch 수용체 배제 매개 [1] | PLD 저해제 사용 시 항암 면역 활성화 [1] |
| Notch 신호 경로 | 대식세포를 친염증성(M1형)으로 재프로그래밍 [1] | 활성화를 통해 종양 내 면역 환경 개선 |
| RBPJ 단백질 | Notch 신호 전달의 최종 단계에서 항암 효과 실현 [1] | Notch 활성화의 필수적인 전사 인자로 작용 |
[개념 쏙쏙] 세포 포식(Efferocytosis)이란?
우리 몸에서는 매일 수십억 개의 세포가 죽습니다. 이 사체들이 방치되면 염증이 생기는데, 대식세포가 이를 깔끔하게 먹어치우는 청소 과정을 ‘세포 포식’이라고 합니다.
이때 대식세포는 주변에 “안심하세요, 평화로운 청소 중입니다”라는 신호를 보내는데, 암세포는 이 평화 신호를 악용해 면역 공격을 피합니다.
이번 연구는 그 평화 신호를 강제로 ‘공격 신호’로 바꾸는 기술을 찾아낸 것이죠.
[개념 쏙쏙] Notch 신호 전달 경로
대식세포(Macrophage)에서 Notch 신호 전달 경로(Notch Signaling Pathway)는 세포의 분화, 활성화 상태(M1/M2 표현형 결정), 그리고 염증 반응 조절에 핵심적인 역할을 합니다
Notch 신호는 전형적인 세포 간 접촉(Cell-to-cell contact) 방식의 신호 전달 체계입니다.
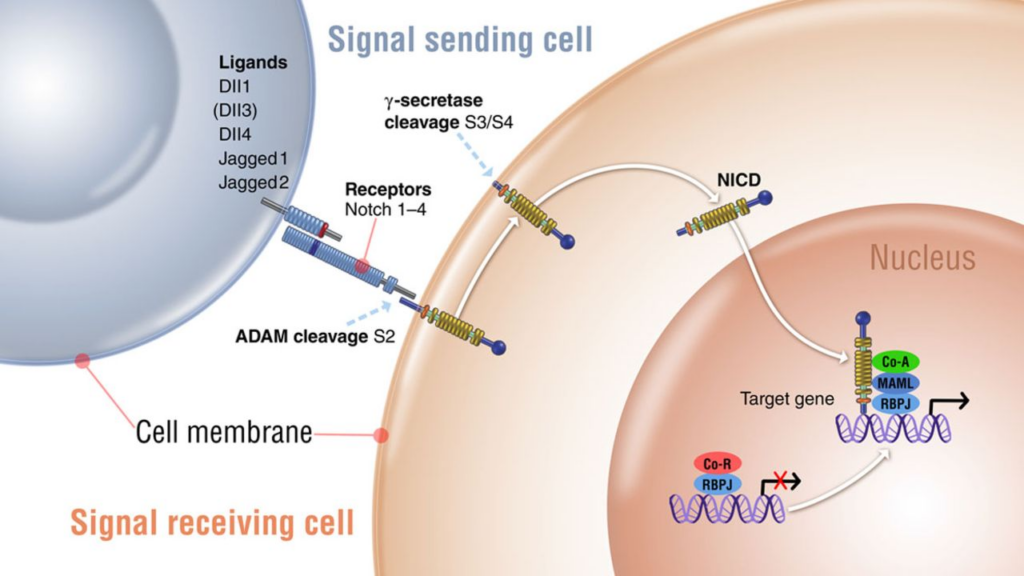
M1 분극화 촉진: Notch 신호의 활성화는 일반적으로 대식세포를 M1(염증성) 표현형으로 유도합니다. 특히 iNOS 발현을 높이고, IL-12, TNF-ą와 같은 염증성 사이토카인 생성을 증가시킵니다
동작 메커니즘: 인접한 세포의 Notch 리간드(DLL1, DLL4, Jagged1, Jagged2)가 대식세포 표면의 Notch 수용체(주로 Notch1, Notch2)와 결합하면, g-secretase 효소에 의해 Notch 수용체의 내측 도메인(NICD, Notch Intracellular Domain)이 절단됩니다.
핵 내 전사 조절: 유리된 NICD는 핵으로 이동하여 전사 인자인 RBP-Jĸ와 결합합니다. 이를 통해 Hes, Hey 패밀리 유전자의 발현을 유도하여 대식세포의 유전자 발현 프로파일을 변화시킵니다.
ID3 단백질과 줄기세포 닮은 T 세포
암 치료에서 가장 큰 난제는 면역 세포들이 암세포와 싸우다 금방 지쳐버리는 ‘면역 탈진(Exhaustion)’ 현상입니다.
Science Immunology 3월호에 실린 Peter Doherty 연구소의 논문은 이 문제를 해결할 ‘면역계의 에너자이저’를 찾아냈습니다.[2, 3]
연구팀은 ‘줄기세포 닮은 T 세포(Stem-like T cells)’라는 희귀한 세포군에 주목했습니다.
이 세포들은 끊임없이 자신을 복제하면서도 지치지 않고 강력한 공격력을 유지하는 능력이 있는데, 그 비결은 바로 ID3라는 유전자가 만드는 단백질에 있었습니다.[2]
ID3 단백질은 T 세포가 암세포의 공격에도 불구하고 번아웃되지 않도록 보호하는 일종의 ‘방열판’ 같은 역할을 합니다.
특히 특정 염증 신호를 주었을 때 이 ID3 단백질을 가진 T 세포들이 폭발적으로 늘어난다는 사실을 확인했는데, 이는 기존 CAR T 세포 치료의 치명적인 단점이었던 ‘짧은 유효 기간’을 획기적으로 늘릴 수 있는 로드맵을 제시한 것입니다.[2, 4]
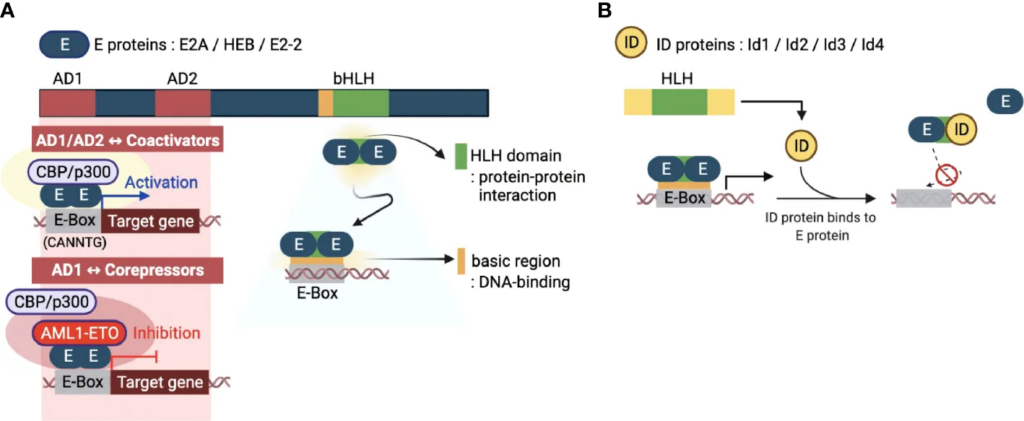
[개념 쏙쏙] ID3 (Inhibitor of DNA Binding 3)
ID3 (Inhibitor of DNA Binding 3) 단백질은 세포의 운명을 결정하는 전사 조절 인자로, 주로 다른 전사 인자의 기능을 억제함으로써 작용합니다.
대식세포를 포함한 면역 세포의 발달과 기능 조절에 있어 매우 중요한 “브레이크” 역할을 수행합니다.
- 구조적 특징: ID3는 HLH(Helix-Loop-Helix) 도메인을 가지고 있지만, DNA에 직접 결합할 수 있는 기본(Basic) 도메인이 결핍되어 있습니다.
- 동작 원리 (Dominant Negative Effect): 정상적인 전사 인자(주로 E-protein 패밀리)는 이량체(Dimer)를 형성하여 DNA에 결합하는데, ID3가 이들과 결합하면 DNA에 붙지 못하는 ‘비활성 복합체’가 형성됩니다. 즉, 특정 유전자의 발현을 차단하는 방식으로 작동합니다.
- 림프구 발달의 필수 요소: B세포와 T세포의 성숙 과정에서 ID3의 농도 조절은 생존과 분화를 결정하는 핵심 스위치입니다. 특히 T세포 수용체(TCR) 신호가 전달되면 ID3 발현이 급증하여 선택 과정에 관여합니다.
CAR T 세포의 진화
현재 가장 각광받는 항암제인 CAR T 세포도 고형암(폐암, 유방암 등) 앞에서는 힘을 못 쓰는 경우가 많았습니다.
종양 내부의 혹독한 환경 때문에 T 세포가 들어가자마자 무력화되기 때문이죠.
Science Immunology에 실린 또 다른 연구는 이 문제를 해결하기 위해 ‘c-Jun‘이라는 전사 인자에 집중했습니다.[4, 5]
연구 결과, CAR T 세포는 종양에 들어가면 TCF1이라는 핵심 인자를 잃어버리고 급격히 노화된다는 것이 밝혀졌습니다.[4]
연구진은 유전자 조작을 통해 c-Jun을 강제로 많이 만들게 했더니, T 세포가 종양 안에서도 줄기세포 같은 젊음을 유지하며 생존했습니다.[3]
여기에 PD-L1 억제제를 함께 사용하자, 마치 잠자던 거인이 깨어난 것처럼 T 세포들이 종양을 거의 완벽하게 청소하는 결과를 보였습니다.[4]
이는 암 치료의 패러다임이 단순한 ‘공격’에서 ‘면역 세포의 건강 관리‘로 이동하고 있음을 시사합니다.
변화하는 항체
보통 항체는 하나의 타겟(항원)만 잡는 집요한 사냥꾼으로 알려져 있습니다.
하지만 2026년 3월 Science Immunology의 표지를 장식한 연구는 ‘IgG4’라는 항체의 진화를 소개했습니다.[3, 11]
IgG4 항체의 기묘한 변신
이 항체들은 혈액 속을 돌아다니다가 갑자기 자신의 몸을 반으로 쪼갠 뒤, 옆에 있는 다른 IgG4와 팔을 바꿔 끼웁니다.
이를 ‘Fab-arm exchange‘라고 부릅니다.[11]
이 과정을 거치면 하나의 항체가 왼쪽 팔로는 A라는 세균을, 오른쪽 팔로는 B라는 바이러스를 잡을 수 있는 ‘이중 특이성 항체’로 거듭나게 됩니다.[3]
거의 모든 인간의 혈중 IgG4가 이 댄스 파티에 참여하고 있다는 사실이 이번에 처음으로 밝혀졌는데, 이는 우리 몸이 고정된 무기만 쓰는 게 아니라 상황에 맞춰 실시간으로 무기를 조합해 쓰는 아주 영리한 시스템을 갖추고 있음을 보여줍니다.[11]
이 발견은 향후 알레르기 치료나 새로운 백신 설계에 있어 IgG4를 어떻게 활용할지에 대한 완전히 새로운 시각을 제공합니다.
우리가 옥수수를 먹어도 괜찮은 이유
우리가 매일 먹는 음식이 왜 면역 공격을 받지 않는지 궁금해본 적 있나요?
Science Immunology 4월호에 게재될 예정인 연구는 옥수수 단백질인 ‘알파-제인(alpha-zein)’이 우리 장 내 면역 세포를 교육하는 과정을 밝혀냈습니다.[3]
우리 장 속에는 음식을 적으로 오해하지 않게 만드는 ‘조절 T 세포(Treg)’가 있는데, 이들 중 상당수가 옥수수 같은 곡물의 단백질 조각을 인식해 발달합니다.[3]
특히 젖을 떼는 시기(weaning)에 이 조절 T세포들이 집중적으로 만들어지며, 이들이 제대로 형성되지 않으면 나중에 성인이 되어서도 각종 음식 알레르기나 장 염증에 시달릴 수 있습니다.[3]
“골고루 먹어야 건강하다”는 어른들의 말씀이 사실은 “면역 세포를 제대로 교육해야 한다”는 고도의 과학적 조언이었던 셈이죠.
[개념 쏙쏙] 조절 T세포(Regulatory T cell, Treg)
조절 T세포(Regulatory T cell, Treg)는 면역계의 과도한 활성을 억제하여 면역 항상성을 유지하고 자가면역 질환을 방지하는 핵심적인 세포입니다.
1. Treg의 발달 과정 (Development)
Treg는 발생 장소에 따라 크게 tTreg(thymic Treg)와 pTreg(peripheral Treg)로 나뉩니다.
1-1. 흉선 유래 조절 T세포 (tTreg)
- 발생: 흉선(Thymus)에서 T세포 분화 과정 중, 자신의 항원(Self-antigen)에 대해 중간 정도의 높은 친화력(Intermediate-high affinity)을 가진 TCR(T세포 수용체)을 가진 세포들이 선택됩니다.
- 분자적 마커: 전사 인자인 Foxp3의 발현이 Treg의 정체성을 결정하는 가장 중요한 요소입니다.
- 조건: CD28 공동 자극 신호와 IL-2 신호 전달이 Foxp3 발현 유도와 Treg 생존에 필수적입니다.
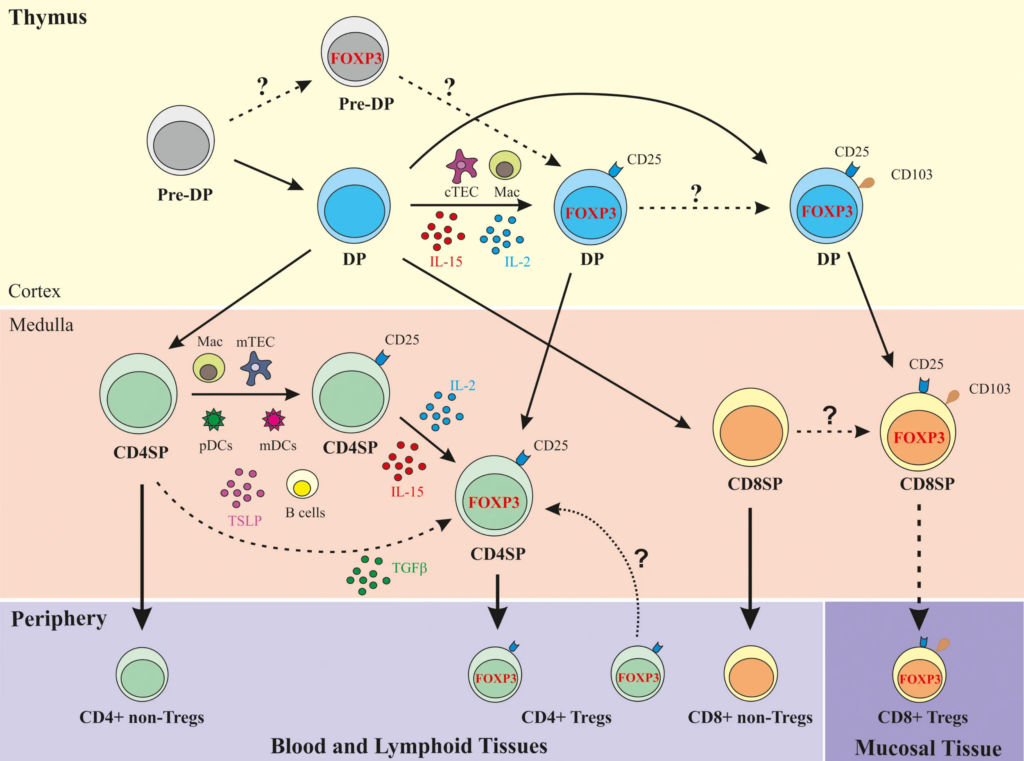
1-2. 말초 유래 조절 T세포 (pTreg)
- 발생: 흉선을 통과한 일반 나이브 CD4+ T세포가 말초 조직에서 특정 환경에 노출될 때 Treg로 분화합니다.
- 역할: 주로 점막 면역(음식물 항원, 장내 미생물 등)에 대한 관용을 유도하는 데 특화되어 있다는 것이 유력한 가설입니다.
2. Treg의 작동 기전 (Functional Mechanisms)
Treg는 어느 하나의 방식이 아니라, 다각적인 ‘면역 억제 칵테일’을 사용하여 주변 면역 세포를 무력화합니다.
- 세포 간 직접 접촉 (Contact-dependent):
- CTLA-4 발현: Treg 표면의 CTLA-4가 수지상세포(APC)의 CD80/86과 결합하여, 일반 T세포가 활성화되는 것을 방해하거나 CD80/86을 제거(Trans-endocytosis)합니다.
- 억제성 사이토카인 분비:
- IL-10, TGF-β, IL-35 등을 분비하여 주변 염증 반응을 직접 억제합니다.
- 대사적 교란 (Metabolic disruption):
- IL-2 기아 (IL-2 Consumption): Treg는 IL-2 수용체(CD25)를 매우 많이 가지고 있어, 주변의 IL-2를 모두 흡수해버립니다. 이로 인해 일반 T세포는 성장에 필요한 IL-2가 부족해져 사멸하게 됩니다. (유력한 가설 및 사실)
- 아데노신 생성: 표면의 CD39, CD73 효소를 통해 ATP를 아데노신(Adenosine)으로 전환하여 면역 억제 신호를 보냅니다.
- 세포 독성: 때로는 Granzyme이나 Perforin을 직접 내뿜어 표적 세포를 사멸시키기도 합니다.
3. Treg의 독특한 역할
- 조직 거주 Treg (Tissue-resident Treg):
- 면역 억제 외에도 비정형적인 기능을 수행합니다.
- 예를 들어 근육 내 Treg는 근육 재생을 돕고, 지방 조직 내 Treg는 인슐린 저항성을 조절하는 대사적 기능을 수행합니다.
- 이는 ‘면역 세포는 면역만 담당한다’는 일반적인 통념의 예외입니다.
- 종양 내 Treg (Intratumoral Treg):
- 고형암 내부의 Treg는 일반적인 Treg보다 훨씬 더 강력한 억제 능력을 갖도록 ‘재프로그래밍’되어 있어, 항암 치료의 가장 큰 방해 요소가 됩니다.
4. CAR-Treg
이는 Treg의 강력한 억제 기능을 특정 부위에만 집중시켜 전신 면역 억제 부작용을 최소화하려는 시도입니다.
최근 과학계는 암을 죽이는 CAR-T를 넘어, 자가면역 질환 치료를 위해 특정 장기만 보호하는 CAR-Treg를 개발하고 있습니다.
구강과 점막 면역의 재발견
Drake Williams 교수팀은 인간의 치아 주변 점막(잇몸 등)을 세포 하나하나 수준에서 지도화한 ‘멀티오믹스 공간 아틀라스’를 완성했습니다.
2026년 3월 Nature Immunology의 표지 논문은 우리의 입속이 단순한 통로가 아니라, 고도로 설계된 ‘면역 요새’임을 보여줍니다.[12]
입속은 지금 24시간 ‘전시 대기’ 상태
연구 결과, 잇몸은 평소에도 미세한 염증 반응이 계속 일어나는 ‘항상성 염증 상태’를 유지하고 있었습니다.[12]
세균이 워낙 많은 곳이라 면역 세포들이 아예 엔진을 끄지 않고 공회전하며 대기하는 상태인 것이죠.[12]
이 지도는 우리가 왜 잇몸 질환(치주염)에 걸리는지, 그리고 입속 건강이 어떻게 전신 면역 질환과 연결되는지를 풀 수 있는 ‘구글 맵’ 같은 역할을 할 것입니다.
질 점막의 문지기: 랑게르한스 세포의 두 얼굴
바이러스가 체내로 들어오는 또 다른 통로인 질 점막에 대한 연구도 발표되었습니다.
Nature Scientific Reports에 실린 연구는 질 점막의 파수꾼인 ‘랑게르한스 세포(LCs)’가 어떻게 HIV 감염의 열쇠를 쥐고 있는지 설명합니다.[13]
평소 미성숙한 상태의 이 세포들은 HIV 바이러스를 잡아먹어 파괴하는 든든한 방어벽입니다.
하지만 주변에 세균 감염이나 염증이 생겨 이 세포들이 활성화되면, 오히려 바이러스를 안전하게 모셔서 체내 깊숙이 전달하는 ‘트로이의 목마’로 변합니다.[13]
특히 질 내 LCs는 피부의 LCs보다 훨씬 더 예민한 감지기(TLR)를 가지고 있다는 사실이 밝혀졌는데, 이는 왜 질 내 염증 관리가 HIV 같은 치명적인 감염 예방에 결정적인지를 과학적으로 입증한 것입니다.
차세대 CRISPR 스크리닝
이제 과학자들은 단순히 면역 세포를 관찰하는 수준을 넘어, 유전자를 마음대로 편집해 최강의 병사를 만들려 하고 있습니다.
Journal of Experimental Medicine(JEM) 3월호에서는 ‘공간 CRISPR 스크리닝‘이라는 신기술을 소개했습니다.[16]
기존에는 세포를 다 갈아서 분석했다면, 이제는 종양 내부 어디에 있는 어떤 T 세포의 유전자를 바꿔야 가장 효과적으로 암을 죽일 수 있는지 ‘위치 정보’를 포함해 분석할 수 있게 된 것이죠.
이는 면역 치료가 ‘대충 쏘는 산탄총’에서 ‘정밀 타격 미사일’로 진화하고 있음을 뜻합니다.
참고자료
- (PDF) Li et al-2026-Nature Immunology – ResearchGate, https://www.researchgate.net/publication/402053323_Li_et_al-2026-Nature_Immunology
- New research unlocks key to long-lasting immune response in cancer and chronic diseases, https://www.doherty.edu.au/articles/new-research-unlocks-key-to-long-lasting-immune-response-in-cancer-and/
- Science Immunology – Read by QxMD, https://read.qxmd.com/journal/53613
- Modulating AP-1 enables CAR T cells to establish an intratumoral …, https://www.researchgate.net/publication/401647249_Modulating_AP-1_enables_CAR_T_cells_to_establish_an_intratumoral_stemlike_reservoir_and_overcomes_resistance_to_PD-1_blockade
- Improving CAR T Cell Responses to Checkpoint Therapy – Immunopaedia, https://www.immunopaedia.org.za/breaking-news/improving-car-t-cell-responses-to-checkpoint-therapy/
- RECOVER Research Update: March 2026, https://recovercovid.org/news/recover-research-update-march-2026
- Immune exhaustion, the culprit for long COVID and chronic complications – PMC, https://pmc.ncbi.nlm.nih.gov/articles/PMC12981522/
- Publications – RECOVER COVID Initiative, https://recovercovid.org/publications
- COVID Timeline | Global Autoimmune Institute, https://www.autoimmuneinstitute.org/covid-timeline/
- Insights into the pathogenesis of rheumatic and immune diseases from single-cell omics, https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2026.1768719/full
- IgG4 on the dance floor: Partners swapped by Fab-arm exchange, https://www.researchgate.net/publication/401647104_IgG4_on_the_dance_floor_Partners_swapped_by_Fab-arm_exchange
- CFI Researcher Drake Williams Featured on Nature Immunology Cover – Medical School, https://med.umn.edu/immunology/news/cfi-researcher-drake-williams-featured-nature-immunology-cover
- The right model for the right virus | Research Communities by Springer Nature, https://communities.springernature.com/posts/the-right-model-for-the-right-virus
- Immune cells may underlie sex differences in chronic pain – NIH, https://www.nih.gov/news-events/nih-research-matters/immune-cells-may-underlie-sex-differences-chronic-pain
- Antimicrobial resistance – a tale of silence and lessons – Microbiology – Nature, http://microbiologycommunity.nature.com/posts/antimicrobial-resistance-a-tale-of-silence-and-lessons
- Next-generation CRISPR screens enable causal systems immunology, https://rupress.org/jem/article/223/3/e20241266/281510/Next-generation-CRISPR-screens-enable-causal
- Measure What (and When it) Matters: Building digital biomarkers for clinical trials, https://communities.springernature.com/posts/58304-measure-what-and-when-it-matters-building-digital-biomarkers-for-clinical-trials